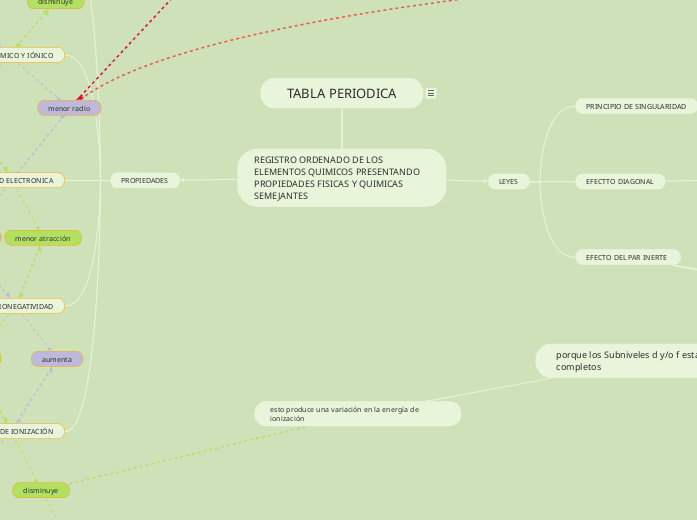
TABLA PERIODICA
REGISTRO ORDENADO DE LOS ELEMENTOS QUIMICOS PRESENTANDO PROPIEDADES FISICAS Y QUIMICAS SEMEJANTES
PROPIEDADES
CARGA NUCLEAR EFECTIVA
ATRACCIÓN DEL NUCLEO SOBRE LOS ELECTRONES
aumenta
Qué le pasa a un elemento si...
disminuye
RADIO ÁTOMICO Y IÓNICO
MITAD DE LA DISTANCIA ENTRE LOS NUCLEOS DE 2 ATOMOS ADYACENTES
mayor radio
menor radio
AFINIDAD ELECTRONICA
ENERGIA QUE SE LIBERA CUANDO SE AÑADE UN ELECTRON A UN ATOMO PARA FORMAR UN ION CON CARGA
mayor atracción
menor atracción
ELECTRONEGATIVIDAD
CAPACIDAD DE UN ÁTOMO DE ATRAER ELECTRONES HACIA SI LOS ELECTRONES EN UN ENLACE QUIMICO
aumenta
disminuye
ENERGIA DE IONIZACIÓN
ENERGIA MINIMA PARA REMOVER UN ELECTRÓN DE UN ÁTOMO POLIELECTRONICO EN ESTADO GASEOSO
disminuye
mayor oxidación
dar ejemplos de alguno de los elementos del grupo 13 o 15
aumenta
menor oxidacion
dar ejemplo del sodio
LEYES
PRINCIPIO DE SINGULARIDAD
ELEMENTOS DEL SEGUNDO PERIODO QUE PRESENTAN CARACTERISTICAS DIFERENTES A LOS ELEMENTOS DE SU MISMO GRUPO
Razones escenciales
Minúsculo tamaño
tendencia a formar enlaces pi
ausencia de orbitales "d"
incapacidad de expandir el octeto
Litio, Berilio, Boro, Carbono, Nitrogeno, Oxigeno, Fluor y Neon
EFECTTO DIAGONAL
CARACTERISTICAS SIMILARES DE LOS ELEMENTOS
EFECTO DEL PAR INERTE
Si un eleme
Subtopic
provocan
Distorsión en su nube electronica
Polarización de los enlaces
Hidratación de la molecula
Carácter covalente
Mayor relación carga - enlace
Movimiento de la densidad electrónica
ELEMENTOS DE LOS GRUPOS III A - V A PIERDEN LA CAPACIDAD DE APANTALLAR LOS ELECTRONES QUE PROTEGEN EL NÚCLEO.
porque los Subniveles d y/o f estan completos
esto produce una variación en la energía de ionización