Scheikunde VWO 4 & VWO 5
H14 Chemie van het leven
H14.2 Koolhydraten
Koolhydraten
sachariden
suikers
Monosachariden en hun structuur
glucose C6H12O6
druivensuiker
Binas tabel 67F1
Monosachariden en reacties
aldose
ketose
Disachariden
hydrolyse
Binas tabel 67F2
2 C6H12O6 -> C12H22O11 + H2O
Polysachariden
cellulose
zetmeel
glycogeen
Binas tabel 67F3
celwanden
SE Bouw van de bekendste polysachariden
cellulose
zetmeel
amylose
amylopectine
glycogeen
Vertering van zetmeel
glucose
fructose
H14.3 Vetten
Oliën en vetten
oliën
vetten
glycerol (propaan-1,2,3-triol)
vetzuren (carbonzuren met een lange koolstofketen)
triglyceriden
vetzuren bestaan uit lange onvertakte ketens met een even aantal C-atomen: 12-, 14-, 16-, en 18-C-atomen komen het meest voor
Bij sommige vetzuren komen één of meer dubbele bindingen voor, de ruimtelijke oriëntatie van de groepen rond de dubbele bindingen is altijd cis-vorm
lipiden
Binas tabel 67G2
onverzadigde vetzuren
Vertering van oliën en vetten
worden door hydrolyse omgezet in glycerol en vrije vetzuren
Functie en toepassingen van oliën en vetten
vormen reservebrandstoffen
zijn nodig voor de vorming van membranen
Omegavetzuren
essentiële vetzuren
omega 3-vetzuren
omega 6-vetzuren
H14.4 Eiwitten
Eiwitten
α-C-atoom
α-aminozuren
Binas tabel 67H1
peptidebinding
dipeptide
eiwitten
proteïnen
De molecuulstructuur van een eiwit
primaire structuur
secundaire structuur
α-helix
β-sheet
H-bruggen
tertiaire structuur
zwavelbruggen
Reacties van eiwitten
hydrolyse
denatureren
enzymen
Functies van eiwitten
biokatalysatoren
essentiële aminozuren
H14.5 DNA en RNA
De celkern
DNA
chromosomen
De molecuulstructuur van DNA
Deoxyribo Nucleic Acid
nucleotidenketens
dubbele helix van DNA
nucleotide
H-bruggen (Binas tabel 71C)
Replicatie
replicatie
RNA
RNA (Ribo Nucleic Acid)
In RNA komt ipv de base thymine (T), de base uracil (U) voor
RNA is een polymeer met een enkele keten, het vormt dus geen dubbele helix
transcriptie
Binas tabel 71E en F
Eiwitsynthese
aminozuurvolgorde
genetische code (tripletcode)
anticodon
translatie
Het menselijk genoom
gen
genoom
Verschillende soorten eiwitten
nonsense-DNA
junk-DNA
Mutaties
redenen voor fouten
- veel fouten worden direct hersteld door speciale enzymen;
- fouten treden op in het junk-DNA. Je merkt niets van deze veranderingen;
- veel fouten treden op in genen die niet geactiveerd zijn (uitstaan);
- als er een fout in een geactiveerd gen optreedt die niet wordt hersteld, blijft de schade vaak tot die ene cel beperkt en blijven gevolgen gering
verschillende soorten mutaties
1. een puntmutatie: er wordt één verkeerde base in het DNA ingebouwd, de complementaire streng verandert mee
2. een deletie: door mutaties kan het ook zijn dat een (groot) deel van het DNA verdwijnt. Meestal is dit het gevolg van een breuk in het DNA. In het DNA kunnen deleties voorkomen, van enkele tot duizenden basenparen. Daardoor kan de totale lengte van het DNA tussen individuen verschillen
3. een duplicatie: hierbij wordt een stukje DNA toegevoegd. Meestal gebeurt dit doordat bij de replicatie van het DNA een stukje 2 keer wordt overgeschreven ipv 1 keer. Er kan een duplicatie plaatsvinden van enkele basenparen, maar ook van duizend of meer basenparen
H14.6 Voeding, stofwisseling en gezondheid
Voedingsstoffen
sporenelementen
vitaminen
Binas tabel 82A
Voorbewerkt voedsel
voedingsmiddelenindustrie -> meer gebruiksgemak, maar vaak niet betere kwaliteit
Functional foods
voedingsmiddelen waaraan stoffen zijn toegevoegd die onze gezondheid zouden moeten bevorderen
H13 Kunststoffen
H13.2 Additiepolymerisatie
Polymeren en monomeren
polymeren
monomeren
additiepolymerisatie
condensatiepolymerisatie
Additiepolymerisatie
stap 1: initiatie
stap 2: propagatie
monomeereenheid
stap 3: terminatie
additiepolymeer
H13.3 Condensatiepolymerisatie
Condensatiereacties
condensatiepolymerisatie
condensatiereactie
hydrolysereacties
Polyester
condensatiepolymeren
polyester
copolymeer
Polyamide
polyamide
amide
amidebinding
H13.4 Eigenschappen van kunststoffen
Thermoplast en thermoharder
thermoplasten
thermoharders
crosslinks
netwerkpolymeer
De flexibiliteit van een kunststof
zijketens
polymerisatiegraad
gemiddelde ketenlengte
gemiddelde molecuulmassa
weekmakers
H12 Molecuulbouw en stofeigenschappen
H12.2 Lewisstructuren
Lewisstructuren
valentie-elektronen
lewisstructuur
octetregel
edelgasconfiguratie
bindend elektronenpaar
niet-bindende of vrije elektronenparen
uitgebreid octet
Lewisstructuur opstellen
Stap 1: Bepaal het aantal valentie-elektronen met behulp van Binas tabel 99
Stap 2: berekenen hoeveel elektronen nodig zijn om alle atomen te laten voldoen aan de octetregel
Stap 3: berekenen hoeveel elektronen je tekortkomt
Stap 4: de elektronen die je tekortkomt om te voldoen aan de octetregel krijgen de atomen door elektronen te delen, die elektronen vormen de bindende elektronenparen
Stap 5: berekenen hoeveel niet-bindende elektronenparen overblijven
Stap 6: Teken de lewisstructuur zodanig dat alle atomen voldoen aan de octetregel
Lewisstructuur opstellen van een ion
rekening houden met lading vh ion
lading vh ion wordt opgeteld bij het aantal valentie-elektronen of ervan afgetrokken
Formele lading
Stap 1: Bepaal het aantal elektronen bij elk atoom van het samengestelde ion, dat is het aantal elektronen in de niet-bindende elektronenparen van dat atoom plus een elektron voor elk bindend elektronen paar rond dat atoom
Stap 2: bepaal het aantal valentie-elektronen van elk atoom
Stap 3: het aantal valentie-elektronen van een atoom min het aantal elektronen bij dat atoom is de formele lading
Stap 4: je zet de formele lading bij elk van de atomen, bij een lading van 1+ of 1- laat je het cijfer weg, omcirkel de formele lading, om verwarring met elektronenparen te voorkomen
VSEPR
omringingsgetal
ruimtelijke bouw van moleculen voorspellen
Dipolen
dipool-dipoolbinding
lineair
180°
2-omringing
gelijkzijdige driehoek (vlak)
120°
3-omringing
tetraëder
109,5°
4-omringing
partiële lading
dipolen
H12.3 Mesomerie
Benzeen en fenol
mesomerie
mesomere grensstructuren
Het opstellen van mesomere grensstructuren
formele lading aangeven in de lewisstructuur en van uit daar elektronenparen te verplaatsen
H12.4 Substitutie- en additiereacties
Substitutiereacties
substitutiereacties
reactiemechanisme
radicaalmechanisme
radicaal
initiatie
propagatie
terminatie
ionair mechanisme
nucleofiel
elektrofiel
Additiereacties
additiereactie
radicaalmechanisme
Stap 1: initiatie
Stap 2: propagatie
Stap 3 terminatie
ionair mechanisme
1,2- en 1,4-additie
1,2-additie
1.4-additie
H12.5 Cis-trans-isomerie
Vrije draaibaarheid
isomeren
structuurisomeren
stereo-isomeren
Cis-trans-isomerie
cis
trans
H12.6 Spiegelbeeldisomerie
Spiegelbeeldisomerie
spiegelbeeldisomeren
Asymmetrisch koolstofatoom
asymmetrisch C-atoom
SE Stereo-isomeren met meer dan één asymmetrisch C-atoom
maximale aantal stereo-isomeren bij n asymmetrische C-atomen is 2^n
H11 Redoxreacties
H11.2 Reacties met elektronenoverdracht
Reacties van zure oplossingen met metalen
redoxreactie
Redoxreacties
halfvergelijking of hafreactie
oxidator
reductor
totaalreactie
Herkennen van redoxreacties
kijken naar deeltjes voor en na de reactie, sprake van elektronenoverdracht -> redoxreactie
H11.3 Redoxkoppels
De edelheid van metalen
geconjugeerde reductor
geconjugeerde oxidator
redoxkoppel
Binas tabel 48
Standaardelektrodepotentiaal
- aflopend als ΔV0 ≥ 0,3 V
- evenwicht als -0,3 V < ΔV0 < 0,3 V
- verloopt niet als ΔV0 ≤ -0,3 V
Oxidator of reductor
oxidator en reductor -> hangt af van de andere deeltjes in het reactiemengsel
Stappenplan
H11.4 Redoxreacties in oplossing
Zuur, basisch of neutraal milieu
Binas tabel 48
HSO4^- en SO4^2- zijn alleen oxidator en geconcentreerd zwavelzuur, bij verdund salpeterzuur ontstaat er NO(g), bij geconcentreerd salpeterzuur ontstaat er NO2(g)
Zelf halfreacties opstellen
1. Noteer de gegeven deeltjes
2. Stel de halfreactie van de deeltjes op.
Zuur milieu: voor de pijl H^+ en eventueel H2O als hulpdeeltjes, na de pijl mag geen OH^- ontstaan
Basisch milieu: voor de pijl OH^- en eventueel H2O als hulpdeeltje, na de pijl mag geen H^+ ontstaan
Neutraal milieu: voor de pijl H2O als hulpdeeltje, na de pijl mag H^+ of OH^- ontstaan
3. Maak de deeltjes in de halfreactie kloppend
4. Maak de lading in de halfreactie kloppend door het juiste aantal elektronen (e^-) toe te voegen
H11.5 Alcoholen als reductor
Alcoholen
3 groepen alcoholen
primaire
secundaire
tertiaire
Alcoholen en reductor
primaire en secundaire alcoholen en aldehyde zijn reductoren
primaire alcohol reageert met oxidator -> aldehyde
secundaire alcohol reageert met oxidator -> keton
aldehyde reageert met oxidator -> carbonzuur
H10 Analysetechnieken en onderzoek
H10.2 Spectroscopie SE
Elektromagnetische straling
elektromagnetische straling
golflengte
fotonen
Spectra
spectrum
spectroscopie
absorberen van elektromagnetische straling
uitzenden van elektromagnetische straling
absorptiespectrum
emissiespectrum
Energieniveaus
grondtoestand
aangeslagen toestand
Fotochemie
fotochemische reacties
H10.3 Spectrofotometrie SE
Infrarood spectrofotometrie
sterkvibratie
buigvibratie
ir-spectrofotometrie
Analyse van een ir-spectrum
Binas tabel 39C1 en C2
golflengte
Colorimetrie
colorimetrie
H10.4 Kwantitatieve analyse met spectrofotometrie SE
De spectrofotometer
spectrofotometer
Kwanititatieve analyse met colorimetrie
kwalitatieve analyse
kwantitatieve analyse
monster
blanco
transmissie T
T = I / I0
extinctie
IJklijn
ijklijn
standaardoplossingen
ijkreeks
H10.5 Chromatografie
Papierchromatografie
papierchromatografie
mobiele fase
stationaire fase
chromatogram
Rf-waarde
Rf = afstand van startlijn tot middelpunt van een vlek / afstand van startlijn tot vloeistoffront
Principe van de scheiding
verdelingsevenwicht
Kolomchromatografie
vloeistofchromatografie
gaschromatografie
retentietijd
tR
vloeistofchromatografie
gaschromatografie
Analyse van het chromatogram
kwalitatieve analyse
kwantitatieve analyse
H10.6 Massaspectrometrie
Meten met massaspectrometrie
massaspectrometrie
massaspectrometer
massaspectrum
De massaspectrometer
m/z
Radicalen
radicaal
ongepaard elektron
Massaspectrum
massaspectrum
Kwalitatieve analyse
structuur van moleculen is af te leiden uit een massaspectrum
Kwantitatieve analyse
Uit de piekhoogtes in een massaspectrum kun je de verhoudingen tussen de hoeveelheden van de verschillende deeltjes bepalen
H9 Basen
H9.2 Basen in water
Basen
basische oplossing
pH groter dan 7
Sterke en zwakke basen
zwakke base
geconjugeerd zuur-basepaar
sterke base
H9.3 Formules en namen van basen
Ionen als basen
Binas tabel 49
Binas tabel 45A
een goed oplosbaar zout met een sterk basisch ion
zout reageert direct aflopend met water
1 reactievergelijking
een slecht oplosbaar zout met een sterk basisch ion
geen reactie met water
een goed oplosbaar zout met een zwak basisch ion
2 reactievergelijkingen
1 van de oplossing van het zout
1 van de reactie van de base met water
een slecht oplosbaar zout met een zwak basisch ion
geen reactie met water
meer waardige basen
meer waardige zwakke base
Moleculaire stoffen als base
aminen
zwakke organische basen
ammoniak
zwakke base
eenwaardige base
1 H+-ion opnemen
meerwaardige base
meerdere H+-ionen opnemen
Notaties van basische oplossingen
H9.4 pH-berekeningen aan basische oplossingen
De pOH
pH = -log[H3O+]
pOH = -log[OH-]
[OH-] = 10^-pOH
pH + pOH = 14
Het waterevenwicht
waterconstante
Kw
1,0 x 10^-14 bij 298K
Binas tabel 50
De pH van een oplossing van een sterke base
pOH meteen berekenen uit de molariteit van de oplossing, dan pH berekenen
De pH van een oplossing van een zwakke base
baseconstante
Kb
Binas tabel 49
H9.5 Reacties tussen zuren en basen
Zuur-basereacties
zuur-basereacties
opstellen van een reactievergelijking van een zuur-basereactie
Stap 1: Noteer de formule van alle deeltjes die aanwezig zijn
Stap 2: Bepaal welk deeltje het zuur is en welk deeltje de base
Stap 3: Stel de reactievergelijking van de reageerende deeltjes op
H9.6 Kwantitatieve analyse
Een zuur-basetitratie
equivalentiepunt
eindpunt van de titratie
Titratie van een zwak zuur of base
zwak zuur met sterke base
pH boven de 7 bij het equivalentiepunt
sterk zuur met zwakke base
pH onder de 7 bij het equivalentiepunt
sterk zuur met sterk zuur
pH rond de 7 bij het equivalentiepunt
Nauwkeurigheid van het glaswerk
volpipet
buret
maatkolf
H8 Zuren
H8.2 De pH van een oplossing
Zuur, basisch of neutraal
indicatoren
zuur
basisch
neutraal
zuurgraad
Indicatoren
lakmoes
universeel indicatorpapier
oplossingen
H8.3 Zuren in water
Stroomgeleiding zure oplossing
oxoniumion
Verschil in stroomgeleiding van zure oplossingen
sterk zuur
zwak zuur
Notaties van zure oplossingen
H8.4 Formules en namen van zuren
Organische zuren
organische zuren
zuurrestion
meerwaardige zuren
Anorganische zuren
anorganische zuren
instabiele zuren
Ionen als zuren
Binas tabel 49
H8.5 pH-berekeningen aan zure oplossingen
De pH
pH = -log[H3O+]
[H3O+] = 10^-pH
significante cijfers
De pH van een oplossing van een sterk zuur
pH meteen berekenen uit de molariteit van de oplossing
De pH van een oplossing van een zwak zuur
zuurconstante
Kz
Rekenen aan zwakke zuren
molariteit van het zuur berekenen als pH en Kz gegeven zijn, Kz kan je berekenen als de pH en de molariteit gegeven zijn
H1 Scheiden en reageren
H1.2 Zuivere stoffen en mengsels
Zuivere stoffen
moleculen
element
verbinding
Mengsels
smeltpunt
kookpunt
smelttraject
kooktraject
Verschillende soorten mengsels
oplossing
suspensie
emulsie
tweelagensysteem
hydrofiel
hydrofoob
Emulgator
emulgator
staart
kop
H1.3 Scheidingsmethoden
Scheiden van een mengsel
scheiden
sorteren
stofeigenschappen
verschil in deeltjesgrootte
filtreren
filtraat
residu
verschil in dichtheid
bezinken
verschil in kookpunt
kookpunt
indampen
destillatie
residu
destillaat
destillatieopstelling
verschil in oplosbaarheid
extraheren
extractiemiddel
verschil in adsorptievermogen
adsorptie
adsorptiemiddel
Verschil in adsorptievermogen en oplosbaarheid
papierchromatografie
adsorberen
Rf-waarde
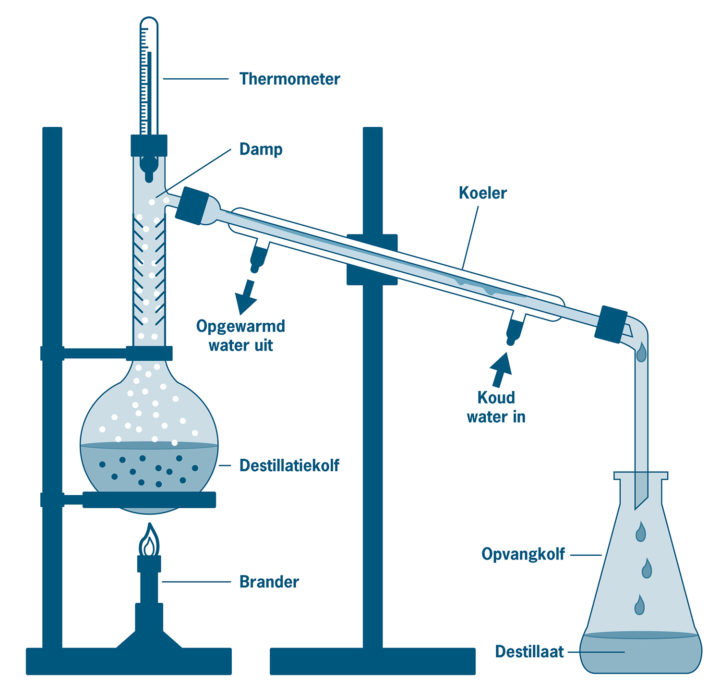
destillatieopstelling
H1.4 Chemische reacties
Kenmerken van een chemische reactie
Beginstoffen worden reactieproducten
Wet van massabehoud
Stoffen reageren en ontstaan in een vaste massaverhouding
Reactietemperatuur
Energie-effect
Het energie-effect van een reactie
chemische energie
Exotherm, energie afstaan aan de omgeving
Endotherm, energie opnemen van de omgeving
faseveranderingen
oplossen
Activeringsenergie
activeringsenergie
Energiediagram
geactiveerde toestand
aflezen van activeringsenergie en reactie-energie
H1.5 De snelheid van een reactie
Reactietijd en reactiesnelheid
Reactietijd
Reactiesnelheid
Welke factoren bepalen de snelheid van een reactie?
1. de soort stof
2. temperatuur
3. de concentratie(s) van de reagerende stof(fen)
4. de verdelingsgraad van een stof
5. de katalysator
enzym
H1.6 Botsende-deeltjesmodel
Effectieve botsingen
effectieve botsing
botsende deeltjesmodel
Modelvoorstelling van een reactie
invloed van de concentratie
Als de concentratie van de beginstoffen kleiner wordt, dan neemt het aantal effectieve botsingen af en dus ook de reactiesnelheid
homogene mengsels
invloed van de temperatuur
Als de temperatuur van de beginstoffen hoger wordt, neemt het aantal effectieve botsingen toe en dus ook de reactiesnelheid
aantal botsingen
heftiger
invloed van de verdelingsgraad
Als de verdelingsgraad van de beginstoffen groter wordt, neemt het aantal effectieve botsingen toe en dus ook de reactiesnelheid
heterogene mengsels
Activeringsenergie en reactiesnelheid
invloed van de soort stof
geactiveerde toestand
aard van de beginstoffen
invloed van een katalysator
katalysator
reactie-energie
H2 Bouwstenen van stoffen
H2.2 De bouw van een atoom
Atoommodellen
Atoommodel Dalton: atoom is massief bolletje. Elke atoomsoort heeft zijn eigen afmetingen.
Atoommodel van Rutherford
Het atoommodel volgens Rutherford: • Een atoom bestaat uit een positief geladen kern en een negatief geladen elektronenwolk. • De atoomkern bestaat uit positief geladen protonen en ongeladen neutronen. • De elektronenwolk bestaat uit negatief geladen elektronen. • Het aantal protonen in een atoom is gelijk aan het aantal elektronen. • Elk atoom heeft een atoomnummer. Alle atomen van dezelfde soort hebben hetzelfde atoomnummer. Het atoomnummer is gelijk aan het aantal protonen. • Elk atoom heeft een massagetal. Atomen van dezelfde soort kunnen verschillende massagetallen hebben. Het massagetal is gelijk aan het aantal protonen + het aantal neutronen
Atoommodel van Bohr
elektronenschillen
elektronenconfiguratie
Isotopen
atomen met zelfde aantal protonen maar verschillende neurtronen
H2.3 Het periodiek systeem
Rangschikking van atoomsoorten in een periodiek systeem
elementen
periodiek systeem
Huidig periodiek systeem
periode
groep
groep 1: alkalimetalen
groep 2: aardalkalimetalen
groep 17: halogenen
groep 18: edelgassen
Atoommodel van Bohr en periodiek systeem
elektronenconfiguratie
H2.4 Ionen, deeltjes met lading
Ionen
positieve ionen
negatieve ionen
Elektrovalentie
positieve elektrovalentie
negatieve elektrovalentie
Elektrovalentie en periodiek systeem
valentie-elektronen
Octetregel
edelgasconfiguratie
octetregel
H2.5 Massa van atomen, moleculen en ionen
Atoommassa
atomaire massa-eenheden
u
atoommassa
massagetal
Gemiddelde atoommassa
1. de massa's van de afzonderlijke magnesium-isotopen;
2. de percentages waarin de verschillende isotopen in het isotopenmengsel voorkomen
Ionmassa en molecuulmassa
ionmassa
molecuulmassa
Rekenen in de scheikunde
meetwaarde
telwaarde
H2.6 Een nieuwe eenheid: de mol
Grootheden en eenheden
grootheid
eenheid
internationaal stelsel van eenheden
SI
afgeleide eenheden
De mol
hoeveelheid stof
n
mol
getal van Avogadro
N^A
H3 Moleculaire stoffen
H3.2 De Bouw van stoffen
Stroomgeleiding
3 groepen
1. Stoffen zowel in de vaste als in de vloeibare fase stroom geleiden (formules met alleen metaalatomen, metalen)
2. Stoffen die alleen in de vloeibare fase elektrische stroom geleiden (formules met combinaties van een metaalatoom met een atoom van een of meer niet-metalen voorkomen, zouten)
3. Stoffen die niet in de vaste en ook niet in de vloeibare fase elektrische stroom geleiden (formules met alleen niet-metalen, moleculaire stoffen)
De bouw van vaste stoffen
kristalrooster
Metalen
metalen
metaalrooster
metaalbinding
Zouten
zout
ionbinding
ionrooster
Moleculaire stoffen
moleculaire stof
vanderwaalsbinding
molecuulrooster
H3.3 Binding in moleculen
Naamgeving van moleculaire stoffen
Binas tabel 66C
1. voorvoegsel voor index
2. naam van de atoomsoort
3. eindigt op -ide
Atoombindingen
atoombinding
covalente binding
covalentie
Lewisstructuren en structuurformules
Lewisstructuur
structuurformule
Polaire en apolaire atoombindingen
apolair
polair
elektronegativiteit
H3.4 Vanderwaalsbinding
Faseovergangen en verderwaalsbinding
1. De aantrekkingskracht tussen de moleculen zorgt voor de vanderwaalsbinding
2. Een hogere temperatuur houdt in dat moleculen heftiger bewegen, temperatuurbeweging
H3.5 Waterstofbruggen
Kookpunten en molecuulbouw
O-H- of N-H bindingen hebben een hogere kookpunt dan je zou verwachten op grond van molecuulmasssa
Water als polair molecuul
polair
dipoolmoleculen
dipool-dipoolbinding
Waterstofbruggen
waterstofbrug
Apolaire moleculen
apolair
H3.6 Mengsels van moleculaire stoffen
Oplossen
hydrofiele stoffen
hydrofobe stoffen
Dynamisch evenwicht
evenwicht
dynamisch evenwicht
verdelingsevenwicht
H3.7 Volume van een mol gas
Volume van een mol gas
wet van Avogadro
Significante cijfers
Significante cijfers
meetwaarde
Rekenen aan het volume van een mol gas
molaire volume (Vm)
H3.8 Percentage, promillage en ppm
Gehalte weergeven
volumepercentage
percentage
promillage
parts per million
H4 Zouten en zoutoplossingen
H4.2 Zouten
Vorming van een zout
reactie niet metaal + metaal --> zout
metaalatomen staan 1 of meer elektronen af aan de niet-metaalatomen
gerangschikt in een ionrooster
De Ionbinding
komt voor in ionrooster als gevolg van elektrostatische krachten tussen de geladen ionen, ionbinding sterker dan waterstofbrug, daarom hoog smeltpunt en kookpunt
H4.3 Namen en formules van zouten
De ionen
enkelvoudige ionen
samengesteld ion
Namen en formules van zouten
systematische naam
triviale namen
triviale naam
Zoutformules
verhoudingsformule
H4.4 Zouten in water
Water als oplosmiddel voor zouten
hydratatie
(aq)
Oplossen en indampen
Oplossen van zouten
oplosvergelijking
Indampen van zoutoplossingen
indampvergelijkingen
Oplosbaarheid
geleidingsvermogen
oplosbaarheid
verzadigd
onverzadigd
Metaaloxiden en water
Binas tabel 45A
'r'
H4.5 Zouthydraten
Kristalwater
kristalwater
zouthydraten
exotherm
endotherm
Toepassingen van zouthydraten
Botbreuken
Droogmiddel
Bouwmaterialen
H4.6 Glaswerk en nauwkeurigheid
SE Glaswerk
volumetrisch glaswerk
Toevallige en systematische fouten
1. toevallige fout
2. systematische fout
Samenvatting significante cijfers
1. Telwaarde hebben geen invloed op de nauwkeurigheid van het antwoord
2. Bij optellen en aftrekken is het aantal cijfers achter de komma van een uitkomst gelijk aan het kleinste aantal cijfers achter de komma waarmee de berekening is uitgevoerd
3. Bij vermenigvuldigen en delen heeft de uitkomst van de berekening evenveel significante cijfers als de gemeten waarde met het kleinste aantal significante cijfer
4. Nullen waarmee een getal begint zij nooit significant
H4.7 Molariteit
Molariteit
aantal mol opgeloste stof / aantal liter oplossing
H5 Reacties van zouten
5.2 Neerslagreacties
SE Het gebruikt van de oplosbaarheidstabel
Binas tabel 45A
SE Neerslagreacties
neerslagreactie
neerslagvergelijking
Dynamisch evenwicht
dynamisch evenwicht
chemisch evenwicht
heterogeen evenwicht
homogeen evenwicht
5.3 Rekenen aan reacties
Rekenen aan reacties
stoichiometrische verhouding
overmaat
SE 5.4 Toepassingen van neerslagreacties
1. een ionsoort verwijderen uit een oplossing; 2. een zout maken; 3. een ionsoort aantonen in een oplossing
Het verwijderen van ionen uit een oplossing
neerslagreactie gebruiken om ongewenste ionen uit een oplossing te verwijderen, neerslag filtreert af, filtraat kan geloosd worden
Het maken van zouten
Slecht oplosbaar zout --> samenvoegen 2 oplossingen die ionsoorten bevatten van een zout dat je wil maken en 2 andere ionsoortenn, die geen neerslag geven, gevormde neerslag --> zout
goed oplosbaar zout --> dezelfde manier, maar ionsoorten reageren niet, na filtreren damp je het filtraat in
Het aantonen van ionen in een oplossing
oplossing toevoegen met ion dat reageert met de aan te tonen ionsoort
Ontstaan van hard water
Veel Ca2+ (aq) en/of Mg2+-ionen (aq), hoe hoger de concentraties van deze ionen des te harder het water
Ontharden van hard water
Hard water geeft problemen als het wordt verwarmd, om hard water te ontharden, kun je natronloog toevoegen
H6 Koolstofverbindingen
H6.2 Koolwaterstoffen
Koolwaterstoffen
organische chemie
onvertakte en vertakte koolwaterstoffen
onvertakt
vertakt
homologe reeks
homologe reeksen
alkanen
Structuurformules en isomerie
isomerie
isomeren
- verzadigde koolwaterstoffen;
- onverzadigde koolwaterstoffen;
- cyclische koolwaterstoffen;
- aromaten
Verzadigde en onverzadigde koolwaterstoffen
verzadigde koolwaterstoffen
verzadigd
alkanen
onverzadigde koolwaterstoffen
onverzadigd
alkenen
alkynen
Cyclische koolwaterstoffen
cycloalkanen
cyclische verbinding
acyclisch, niet-cyclisch
Aromaten
benzeen
aromatisch
alifatische koolwaterstoffen
H6.3 Systematische naamgeving
Systematische naamgeving van alkanen
naamgeving van onvertakte alkanen
naamgeving van vertakkingen
alkylgroepen
Regels voor de naamgeving van alkanen
1. Zoek de langste onvertakte keten van C-atomen op --> hoofdketen
2. De stamnaam van het alkaan wordt de naam van het onvertakte alkaan, dat evenveel C-atomen heeft als de hoofdketen
3. Nummer de C-atomen van de langste keten om de plaats te bepalen van de zijgroepen. Het nummeren van de hoofdketen kan van recht naar links of omgekeerd
4. Elke zijgroep wordt vóór de naam van de hoofdketen vermeld, voorafgegaan door het nummer van het C-atoom waaraan deze vastzit.
5. Komt eenzelfde zijgroep vaker voor, gebruik voorvoegsels di (2 keer), tri (3 keer), tetra (4 keer)
6. Bij meerdere zijgroepen wordt de alfabetische volgorde aangehouden
7. In de naam van het alkaan worden getallen gescheiden door een , en tussen een getal en een letter komt een -
Alkenen en alkynen
1. de uitgang van de naam is niet -aan, maar -een;
2. de plaats van een dubbele binding wordt aangegeven met een cijfer
Alkadiënen
alkadieen
Alkynen (CnH2n-2)
Cycloalkanen
cycloalkenen
Aromaten
fenyl
H6.4 Halogeenverbindingen, ethers en alcoholen
Karakteristieke groepen
karakteristieke groep
klasse
hoofdgroep
Halogeenverbindingen
substitutie
additie
Ethers
alkoxyalkanen
Alcoholen
alcoholen
alkanolen
Binas tabel 66D
Fenolen
fenolen
achtervoegsel -ol
voorvoegsel hydroxy-
H6.5 Aldehyden, ketonen en carbonzuren
Aldehyden en ketonen
aldehyden
alkanalen
achtervoegsel -al
voorvoegsel -oxo
ketonen
alkanonen
achtervoegsel -on
voorvoegsel -oxo
Carbonzuren
alkaanzuren
-zuur
-carbonzuur
vetzuren
H6.6 Esters
Esters
alkylalkanoaten
Oliën en vetten
oliën
vetten
glycerol
vetzuren
triglyceriden
onverzadigde vetzuren
H6.7 Aminen en aminozuren
Aminen
achtervoegsel -amine
voorvoegsel amino-
Aminozuren
Binas tabel 67H
H7 Duurzaamheid
H7.2 Fossiele brandstoffen
Energieleveranciers
verbrandingswarmte
Leverancier van grondstoffen
fracties
gefractioneerde destillatie
Thermische kraken
Katalytisch reformen
Milieuproblemen
Koolstofdioxide
Zwaveldioxide
zure regen
rookgasontzwavelingsinstallaties
Stikstofoxiden
H7.3 Biobrandstoffen
Koolstofkringloop
fotosynthese
koolstofkringloop
elementenkringloop
CO2-neutraal
Eerste generatie biobrandstoffen
biobrandstoffen
biomassa
bio-ethanol
biodiesel
omestering
blokschema
stofstromen
reactoren
Tweede generatie biobrandstoffen
biogas
Derde generatie biobrandstoffen
Algen
Zeewier
H7.4 Duurzame ontwikkelingen
Duurzaam
1. economisch haalbaar
2. goed voor het milieu
3. goed voor de mens (sociaal-cultureel)
4. rekening houden met belangen van de toekomstige generateis
Duurzame energie
windenergie
zonne-energie
energie uit water
blauwe energie
geothermische energie
Duurzame kringlopen
stoffenkringlopen
duurzame kringloop
Cradle to Cradle
recyclen
downcyclen
upcyclen
Duurzaam ondernemen en consumeren
duurzame ondernemen
people
planet
profit
duurzaam consumeren
H7.5 Evenwichten
Evenwichtsreacties
chemisch evenwicht
evenwichtsreacties
insteltijd
homogeen evenwicht
heterogeen evenwicht
De evenwichtsvoorwaarde bij een homogeen evenwicht
concentratiebreuk
evenwichtsconstante
K
evenwichtsvoorwaarde
De evenwichtsvoorwaarde bij een heterogeen evenwicht
vaste stoffen staan niet in de concentratiebreuk van een heterogeen evenwicht
Oplosevenwicht en verdelingsevenwicht
verdelingsevenwicht
Kv
oplosevenwicht
Ks
H7.6 Verschuiving van een chemisch evenwicht
Invloed van de concentratieverandering
door toevoegen van beginstoffen verschuift het evenwicht naar de kant van de reactieproducten
Invloed van volume verandering
bij volumeverkleining verschuift het evenwicht naar de kant met de minste deeltjes, bij volumevergroting naar de kant met de meeste deeltjes
Invloed van en katalysator
geen invloed op de samenstelling van het evenwichtsmengsel
Invloed van temperatuur
verandert de waarde van de evenwichtsconstante K
Aflopen van een evenwicht
aflopend evenwicht