Química.
Materia.
Todo lo que ocupa un espacio.
Sustancia Pura
No se descompone.
Elemento.
Compuesto.
Dos o mas elementos diferentes.
Mezclas.
Homogenea
Heterogenea
Métodos de separación.
Decantación.
Filtración.
Evaporización.
Destilación.
Centrifugación.
Cromatografía.
Magnetismo.
Tamizado.
Propiedades
Fisicas.
No se altera la estructura interna
perceptibles con los sentidos.
Tipo
Intensiva.
Extensiva.
Depende de la cantidad.
Químicas
Alteración de la estructura interna
Combustión.
Oxidación.
Descomposición.
Estados.
Sólido.
Líquido.
Gaseoso.
Plasma.
Conversión de unidades.
Transformación de magnitudes físicas.
A valores equivalentes.
en otra unidad de medida
por medio
Factores de conversión.
como
Longitud.
Volumen.
Masa.
Área.
Presión.
Tiempo.
Estructura Atómica.
Átomo.
Cantidad mas pequeña de un elemento.
Conformación atómica.
Protones.
Electrones.
Neutrones.
Partículas subatómicas.
Elemento.
Número.
Atómico
Número de protones
Masa
Suma neutrones y protones.
Isótopo
Igual número atómico, diferente masa atómica.
Iones
Gana electrones
Carga negativa
Anión
Pierde electrones.
Carga positiva
Catión
Subtema
Número cuántico.
principal
Niveles de energía
n
Secundario
n-1=)(
1-1=0>s
2-1=1>p
3-1=2>d
4-1=3>f
Magnético
Forma orbital
m
Spin
Sentido del giro del e~
Tabla periódica.
propiedades
Radio covalente
Radio atómico
Radio iónico
Afinidad electrónica
Energía de ionización
Electronegatividad
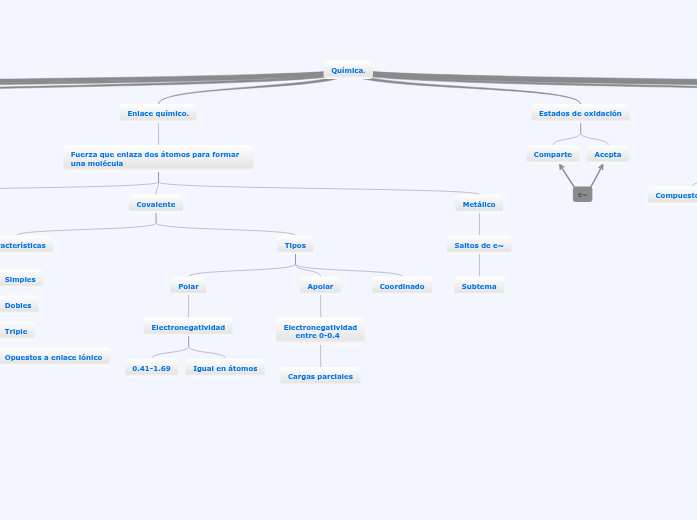
Enlace químico.
Fuerza que enlaza dos átomos para formar una molécula
Enlace iónico
Electronegatividad
>1.7
Características
Sólidos cristalinos
Conductores de electricidad
Altos puntos de fusión y ebullición
Solubles en agua
Covalente
Características
Simples
Dobles
Triple
Opuestos a enlace iónico
Tipos
Polar
Electronegatividad
0.41-1.69
Igual en átomos
Apolar
Electronegatividad
entre 0-0.4
Cargas parciales
Coordinado
Metálico
Saltos de e~
Subtema
Estados de oxidación
Comparte
Acepta
Funciones químicas inorgánicas
Óxido
Compuesto binario
Presencia de
oxigeno
Base o hidróxido
MO + H2O > M(OH)x
Ácidos
Características
Presencia inicial de H
No metales
Tipos
Óxacido
H + NM + O2> HxNMOy
Hidrácidos
NM + H2 > HNM
Sales
Tienen un metal y no metal
Tipos
Oxisal
MNMO
Halogenas
Binarias
Hidruros
Estado de oxidación H
-1
Nomenclatura
Tipos
Sistematica
Prefijos
Mono
Di
Tri ...
Stock
Función qca.
+ elemento
+ estado de oxidación
IUPAC o Tradicional
Según estados de oxidación
-- Hipo~oso
-~oso
+~ico
++ Per~ico
+++ Hiper~ ico
Tipos de reacciones
Síntesis o combinación
A+B>AB
Descomposición
AB>A+B
Sustitución simple
AB+C>AB+B
Sustitución doble
AB+CD>AC+BD
Combustión
corg+O2>CO2+H20+/\
Balanceo
Ley de la conservación de la materia
Pasos
*metales
*no metales
*hidrógeno
*oxígeno *
Tanteo
Estequiometría
Relación cuantitativa
Composición porcentual
Relaciona
Peso compuesto
Peso total de la molécula
Tipos de reactivo
Exceso
No reacciona completamente
Límte
Determina la reacción
Pasos
*Balancear
*Determinar pureza
*Establecer R. Límite
*Rendimiento teórico
*% de rendimiento
Soluciones
Composición
Soluto
se disuelve
Solvente
Medio dispersor
Tipos
Insaturada
+solvente
Sobresaturada
+soluto
Saturada
Cantidad ideal
Solubilidad
capacidad de disolverse
Factores que afectan
Superficie de contacto
Temperatura
Presión
Agitación
Naturaleza
Unidades de concentración
Relación soluto-solución
masa-masa
masa-volumen
volumen-volumen
partes por millon