によって Jenisej Rivera 2年前.
434
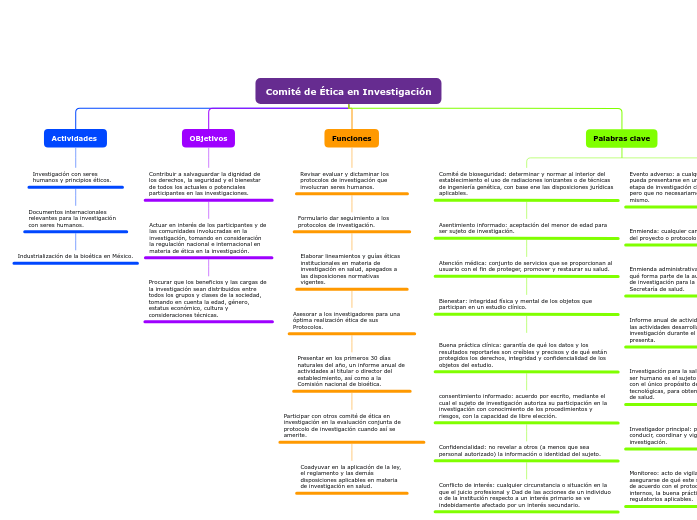
Comité de Ética en Investigación
によって Jenisej Rivera 2年前.
434

もっと見る
Enmienda administrativa: cualquier cambio en un documento qué forma parte de la autorización de un proyecto o protocolo de investigación para la salud en seres humanos emitido por la Secretaría de salud.
Informe anual de actividades: contiene información acerca de las actividades desarrolladas por el comité de ética en investigación durante el ejercicio fiscal anterior al año que se presenta.
Investigación para la salud con seres humanos: en la que el ser humano es el sujeto de investigación y que se desarrolla con el único propósito de realizar aportaciones científicas y tecnológicas, para obtener nuevos conocimientos en materia de salud.
Investigador principal: profesional de la salud, responsable de conducir, coordinar y vigilar el desarrollo de dicha investigación.
Monitoreo: acto de vigilar el proceso de un estudio clínico y asegurarse de qué este sea conducido, registrado y reportado de acuerdo con el protocolo, procedimientos operativos internos, la buena práctica clínica y los requerimientos regulatorios aplicables.
Atención médica: conjunto de servicios que se proporcionan al usuario con el fin de proteger, promover y restaurar su salud.
Bienestar: integridad física y mental de los objetos que participan en un estudio clínico.
Buena práctica clínica: garantía de qué los datos y los resultados reportarles son creíbles y precisos y de qué están protegidos los derechos, integridad y confidencialidad de los objetos del estudio.
consentimiento informado: acuerdo por escrito, mediante el cual el sujeto de investigación autoriza su participación en la investigación con conocimiento de los procedimientos y riesgos, con la capacidad de libre elección.
Confidencialidad: no revelar a otros (a menos que sea personal autorizado) la información o identidad del sujeto.
Conflicto de interés: cualquier circunstancia o situación en la que el juicio profesional y Dad de las acciones de un individuo o de la institución respecto a un interés primario se ve indebidamente afectado por un interés secundario.
Elaborar lineamientos y guías éticas institucionales en materia de investigación en salud, apegados a las disposiciones normativas vigentes.
Asesorar a los investigadores para una óptima realización ética de sus Protocolos.
Presentar en los primeros 30 días naturales del año, un informe anual de actividades al titular o director del establecimiento, así como a la Comisión nacional de bioética.
Participar con otros comité de ética en investigación en la evaluación conjunta de protocolo de investigación cuando así se amerite.
Coadyuvar en la aplicación de la ley, el reglamento y las demás disposiciones aplicables en materia de investigación en salud.
Procurar que los beneficios y las cargas de la investigación sean distribuidos entre todos los grupos y clases de la sociedad, tomando en cuenta la edad, género, estatus económico, cultura y consideraciones técnicas.
Industrialización de la bioética en México.