door Gabriela Saldarriaga 5 jaren geleden
3511
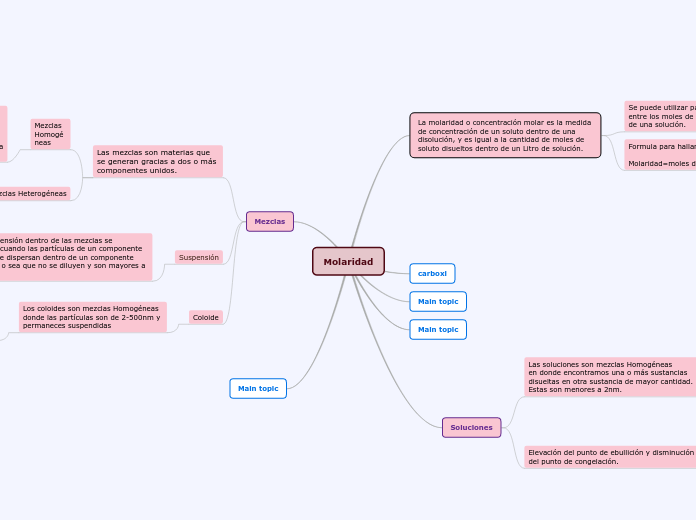
Molaridad
door Gabriela Saldarriaga 5 jaren geleden
3511

Meer zoals dit
Un ejemplo de un Coloide es la gelatina ya que es un polvo que queda suspendido dentro del agua, y al dejarlo en el refrigerador no se va a separar.
Un ejemplo de suspensión es la leche achocolatada cuando vemos que las partículas de chocolate se quedan flotando en la superficie o cuándo quedan acumuladas en el fondo.
A diferencia de las Mezclas Homogéneas, las Mezclas Heterogéneas son aquellas que no tienen una composición uniforme, por lo que sus componentes suelen distinguirse fácilmente.
Un ejemplo de las Mezclas Heterogéneas es agua+aceite, ya que existe una repulsión entre las moléculas de el aceite con las moléculas del agua, lo que hace que no sea posible crear una mezcla uniforme.
Las Mezclas Homogéneas, también conocidas como soluciones son aquellas en donde la composición de las sustancias es uniforme, por lo que distinguir sus componentes a simple vista puede llegar a resultar imposible.
Un ejemplo de este tipo de mezcla es agua+vinagre ya que el vinagre se diluiría completamente en el agua.
Solvente
Es el componente dentro de una solución que se encuentra en mayor cantidad.
Soluto
Es cualquier especie química