realizată de Schulte Martinez Laura 3 ani în urmă
596
PROPIEDADES FÍSICAS Y QUÍMICAS DE LA MATERIA. MODELOS EXPLICATIVOS
realizată de Schulte Martinez Laura 3 ani în urmă
596

Mai multe ca acesta
Ejercicio en el que se aplica la hipótesis de Avogadro
SON DIATÓMICOS TODOS LOS GASES MENOS LOS NOBLES
En mismas condiciones de temperatura y presión, volúmenes iguales tienen el mismo número de partículas
ejemplo
Los volúmenes de los reactivos y la de los productos, en las mismas condiciones de presión y temperatura, guardan una relación de números enteros.
Explicación a partir del ejemplo
Las diferentes masas de los elementos que se combinan con una masa fija del otro, guardan entre sí una relación de números enteros sencillos.
m (reactivo 1) + m (reactivo 2)= m (producto) m (1 y 2)= proporción cte
Cuando 2 o más elementos se combinan, lo hacen manteniendo una proporción de masa constante
Ejemplo
m (reactivos) = m (producto)
La materia NO se CREA NI se DESTRUYE, solo SE TRANSFORMA
T (0K )= Cesa el movimiento
-T=- mov. de partículas
+T=+ mov. de partículas
GASES: ENLACE MUY DEBIL="ROMPE" movimiento total de las partículas
LÍQUIDOS: ENLACE MÁS DEBÍL QUE EL DE LOS SÓLIDOS el movimiento de la partículas es mayor que el de los sólidos
SÓLIDOS: ENLACE FUERTE impide que las partículas se separen, por lo que habrá menor movimiento de partículas
De la fórmula:
y= k
x
k= constante de proporcionalidad.
k= x· y
Type in the subject of your essay.
Composición centesimal (%en masa de cada elemento)
Comparar masa de cada elemento con la masa total del compuesto y multiplicar · 100
Fórmulas
Molecular
Elementos+ exactamente cuántos átomos hay
Empírica
Elementos+ proporción en cómo se combinan
1 MOL de un compuesto, equivale a su MASA MOLECULAR expresada en GRAMOS.
Número de Avogadro
Avogadro:
Mismos volúmenes de distintos gases= mismo número de partículas, por lo tanto:
"1 mol de distintos gases= mismo número de partículas"
MASA MOLECULAR RELATIVA
Suma de las masas atómicas de cada uno de los elementos por cada uno de sus átomos
MASA ATÓMICA RELATIVA *adimensional*
Es la masa de sus átomos en relación a la doceava parte de la masa del átomo de carbono 12.
*se obtiene de la tabla periódica"
Unidad 1u= 1,6605· 10^-27 kg
1unidad (u)= masa que corresponde a la doceava parte del átomo del isótopo del carbono 12.
poca proporción de soluto
gran proporción de soluto
Fracción molar (X)
Molalidad (m)
Molaridad (M)
Fórmula
Ejemplo:
Examples
densidad
Fórmula+ ejemplo
%masa
%volumen
concentración en masa
menor proporción
mayor proporción
DENSIDAD DE LOS GASES IDEALES
Calcular la densidad:
Calcular la masa molar:
En el número de moles (n), interviene la masa (m) y la masa molar (M)
perspective C
EC. ESTADO D E GASES IDEALES
ECUACIÓN:
n moles de un gas cualquiera= R· n (nº de moles)
1 mol de un gas cualquiera= R (constante)= 0,082 atm L/K·mol
EC. GASES IDEALES
GASES cuya T (temperatura) > T (ebullición)
.
UNIDADES:
V= L/m³
P= atm, Pa, mmHg
Presión y Volumen: se puede elegir en que unidades, siempre que sean las mismas
T= K (siempre)
In the main body of your essay, you should list your arguments which will support your thesis.
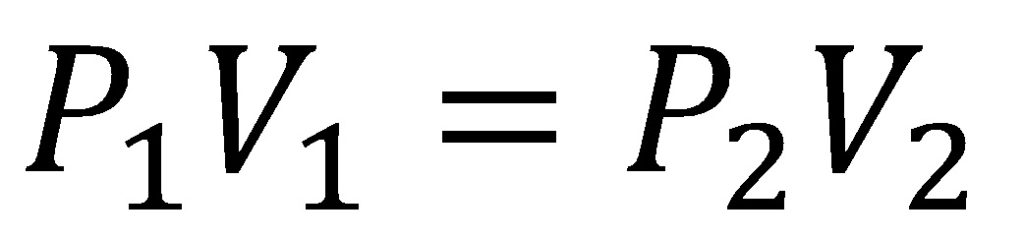
T= cte
Estudia la relación entre V (volumen) y P (presión).
You can choose to argue from different perspectives. For example, you can choose to agree or disagree or remain objective of the main idea.
CONCLUSIÓN-LEY
T

MÉTODO CIENTÍFICO
P= cte
Estudia la relación entre V (volumen) y T (temperatura).
You can choose to argue from different perspectives. For example, you can choose to agree or disagree or remain objective to the main idea.
CONCLUSIÓN-LEY
T

MÉTODO CIENTÍFICO
---
EJEMPLO:
Theory
V= cte
Estudia la relación entre P (presión) y T (temperatura).