por Josue Machuca hace 3 años
184
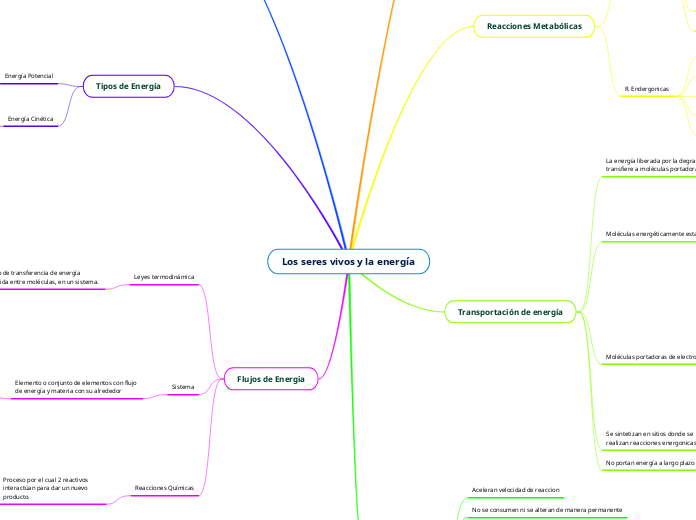
Los seres vivos y la energía
por Josue Machuca hace 3 años
184

Ver más
Tipos de Reacciones
Endergónica
Disminuyen la entropia
Requieren energía
Fotosíntesis
Exergónica
Libera energía
Aumenta la entropía
Tipos
Abierto
Flujo de materia y energía con su alrededor
Digestión
Respiración
Todo esto gracias a la membrana plasmatica
Aislado
No existe el intercambio de materia y energía
Cerrado
Intercambio de energía con su alrededor. No flujo de materia
Subtopic
2°Ley
Aumento de la entropia
Cada transferencia de energia aumenta la entropía del universo
La entropía se contrarresta gracias a la energía emitida por el Sol y los organismos fotosintéticos.
Entropía: grado de desorden, perdida de energía utilizable.
1° Ley:
La energía no se crea ni se destruye, solo se transforma
De el 100% de energía, 25% es energía útil (E. Cinética) y el 75% energía menos útil (E. Térmica)
Relacionado con los enlaces de las macromoléculas
Lípidos
Energía a largo plazo, almacén
Carbohidratos
Mayor fuente de energía, contiene glucosa
FADH
NADH
NADP
NAD
Moneda de intercambio mas abundante
Enlace fosfatoanidrido
∆G > 0
Cuesta arriba
Necesita energía constante
∆G < 0
Cuesta abajo
No necesita energía constante
C6H12O6 + O2 ----> CO2 + H2O (liberando energía ATP)
(-)
Sistema con mayor orden
Espontaneas, no necesitan aporte de energia
Moléculas pequeñas a moléculas grandes
(+)
Sistema mas desordenado durante la reaccion
No son espontaneas, porque necesitan aporte de energía
Moléculas grandes a moléculas pequeñas
∆S
Entropía
Cambia en el sistema durante la reacción
T
°K
∆H
Entalpia
Energía almacenada en los enlaces