作者:Renato Oliveira 5 年以前
568
Revisões 7º ano
作者:Renato Oliveira 5 年以前
568

6 - Depois de analisares o esquema anterior da ENERGIA, responde às questões seguintes:
6.1- Qual é a unidade do SI de energia?
6.2- Quando ocorre uma transferência de energia, como se chama o sistema que recebe a energia?
6.3- Qual é a diferença entre uma fonte de energia renovável e uma não renovável?
6.4- Dá um exemplo de uma fonte de energia renovável e outra de uma fonte de energia não renovável.
6.5- Quais são os dois processos de transferência de energia referidos no esquema?
6.6- Qual dos dois processo de transferência de energia não é necessário haver contacto entre os corpos, isto é, não envolve um meio material?
6.7- Qual é a relação de estudar-se os processos de transferência de energia e a construção das casas?
7- Visualiza o vídeo e responde às seguintes questões:
vídeo: https://reccloud.com/u/8dz6hg3
7.1- A transferência de calor ocorre (escolhe a opção correta).
a) entre corpos com temeperaturas igual.
b) do corpo de maior temperatura para o de menor temperatura.
c) do corpo de menor temperatura para o de maior temperatura.
7.2- Qual é a condição para haver equilíbrio térmico entre dois corpos?
7.3- O que está errado, cientificamente, na expressão que por vezes dizemos no verão ou num dia solarengo: "hoje está muito calor".
Fontes de energia renováveis, quando estão em contínua renovação, podendo ser utilizadas constantemente e considerando-se, por isso, ilimitadas;
Fontes de energia não renováveis, quando a sua reposição, que demora centenas de milhar de anos, é extremamente lenta comparativamente à sua utilização, considerando-se, por isso, limitadas.
Fontes de energia não renovável
Nucleares
• Urânio
• Plutónio
Fósseis
• Petróleo
• Carvão
• Gás natural
Fontes de energia renovável:
Sol
Biomassa: queima de matéria orgânica (resíduos florestais e agrícolas, sólidos urbanos e industriais...)
Biogás: resulta da decomposição de matéria orgânica (resíduos agropecuários e agroindustriais...)
Vento (eólica)
Ondas e marés
Hídricas (água presa nas barragens)
Geotérmicas (calor do interior do planeta Terra)
Células de combustível (resulta de reações químicas do hidrogénio e oxigénio )
ENERGIA
O símbolo da grandeza física energia é a letra E.
Não é fácil dizer o que é a energia. Mas sabemos o que não é!
A unidade SI de energia é o joule. E o símbolo do joule é a letra J.
A caloria também pode ser utilizada como unidade de energia: cal.
1 cal = 4,18 J
vídeo: https://reccloud.com/u/vd579ng
ISOLAMENTO DAS CASAS
vídeo: https://reccloud.com/u/7n9b3iz
Durante o tempo "frio" o calor transfere-se do interior para o exterior das habitações (do sistema de maior temperatura para o de menor temperatura). É por isso que as casas tendem a ficar com menores temperaturas..."frias".
A transmissão de calor faz-se:
• por condução, através dos materiais que constituem, por exemplo, as paredes, o telhado e o chão;
• por convecção, através das frinchas das janelas, das portas e do telhado.
Para minimizar as perdas de energia sob a forma de calor devemos escolher criteriosamente os materiais que melhor contribuem para o isolamento térmico das habitações, recorrendo aos de baixa condutividade térmica.
Processo de transferência de energia
Os processos de transferência de energia podem ocorrer sob a forma de CALOR ou por RADIAÇÃO.
Isso acontece se os sistemas tiverem a temperaturas diferentes.
O processo de transferência ocorre do sistema com maior temperatura para o sistema de menor temperatura.
A transferência termina quando os dois sistemas igualam o valor de temperatura, isto é, atinjem o equilíbrio térmico.
nota: a temperatura está relacionada com a agitação dos corpúsculos que constituem os corpos (chamada agitação térmica).
A temperatura será tanto maior quanto maior for a agitação térmica dos corpúsculos.
A temperatura mede-se com um termómetro e a unidade utilizada no dia a dia é o grau Celsius, cujo símbolo é ⁰C (não é correto dizer graus centígrados).
RADIAÇÃO
vídeo: https://reccloud.com/u/4vbn2kc
A transferência de energia por radiação ocorre através da propagação de ondas eletromagnéticas (luz visível e invisível) que não precisam de qualquer meio material para se propagarem, isto é, não é necessário haver contacto entre os corpos.
exemplo: a transferência de energia através da propagação da luz
(emitida pela fonte de energia como o Sol, lâmpada, etc...)
CALOR
vídeo: https://reccloud.com/u/61je3rl
A transferência de energia como calor que ocorre principalmente nos sólidos faz-se corpúsculo a corpúsculo, lentamente, ao longo de toda a sua extensão, sem que haja movimento global de matéria, e designa-se por condução térmica.
Diferentes materiais implica diferentes formas de condução térmica.
O valor da condutividade térmica de um material indica se o material é bom ou mau condutor: um valor maior significa que o material é melhor condutor térmico. Estes valores encontram-se disponíveis em tbelas de condutividade térmica.
exemplo: os metais são bons condutores térmicos comparado coma madeira
Quando mergulhamos as mãos em água a temperatura diferente:
•temos a sensação de que a água está quente quando há passagem de calor da água para a mão, aumentando a temperatura da mão;
•temos a sensação de que a água está fria quando há passagem de calor da mão para a água, diminuindo a temperatura da mão.
Convecção
vídeo: https://reccloud.com/u/gwne6fp
A convecção é um processo de propagação do calor característico dos gases e dos líquidos. Ocorre movimento global da matéria.
As correntes quentes têm sentido ascendente: sobem.
As correntes frias têm sentido descendente: descem.
exemplos: o ar quente sobe e o ar frio. Saõ estas coreentes de ar em convecção que explicam que certos pássaros conseguem planar (nã batem as asas) e não caiem. Também o desporto de parapente é possível devido às correntes de convecção.
Também numa panela com água a aquecer há movimentos de água ascendente e descendente.
Condução térmica
vídeo: https://reccloud.com/u/1dmhvi3
A transferência de energia sob a forma de calor ocorre principalmente nos sólidos faz-se corpúsculo a corpúsculo.
Acontece lentamente, ao longo de toda a sua extensão, sem que haja movimento global de matéria, e designa-se por condução térmica.
Diferentes materiais implica diferentes formas de condução térmica.
O valor da condutividade térmica de um material indica se o material é bom ou mau condutor: um valor maior significa que o material é melhor condutor térmico. Estes valores encontram-se disponíveis em tabelas de condutividade térmica.
exemplo: os metais são bons condutores térmicos comparado coma madeira
Quando mergulhamos as mãos em água a temperatura diferente:
•temos a sensação de que a água está quente quando há passagem de calor da água para a mão, aumentando a temperatura da mão;
•temos a sensação de que a água está fria quando há passagem de calor da mão para a água, diminuindo a temperatura da mão.
Sistema: é o corpo ou conjunto de corpos que queremos estudar.
A energia transfere-se da FONTE para o RECETOR.
Fonte: é o sistema que cede a energia.
Recetor: é o sistema que recebe a energia.
No final do processo de transferência (num sistema isolado) a energia é sempre a mesma: a energia não se cria nem se destroi, apenas transfere-se entre sistemas.
vídeo: https://reccloud.com/u/pk06ad4
exemplos:
o João come a maçã. Fonte: maçã recetor: o João
pontapé na bola. Fonte: pé do jogador recetor: bola
panela com água a aquecer num fogão: Fonte: fogão recetor: água
5- Considera as seguintes substâncias dentro de um recipiente: grãos de milho, grãos de arroz, grãos de açúcar e limalha de ferro. Os grãos de arroz são do mesmo tamanho dos grãos de açúcar.
5.1- Como classificas esta mistura ?
5.2- Escreve o(s) procedimento(s) que terias de fazer para separar os quatro componentes da mistura.
Quando temos uma mistura podemos usar processos de separação para obter as substâncias constituintes dessa mistura.
Uma das formas é através de processos físicoa.
Manual 7º ano: pág 146 até 153. E página 155.
CENTRIFUGAÇÃO
Técnica que permite depositar pequenos fragmentos sólidos em suspensão num líquido. Para isso utiliza-se uma centrífuga que faz rodar a mistura com grande velocidade.
exemplo: podes utilizar esta técnica para depositar cinza que está em suspensão na água. Posteriormente, consegues separar a cinza da água por decantação.
vídeo Escola Virtual: https://reccloud.com/u/mpywob9
FILTRAÇÃO
- Separar sólidos em suspensão num líquido.
- Consiste em fazer passar a mistura por um filtro que retém o sólido e deixa passar o líquido.
exemplo: separar pó da água.
vídeo Escola Virtual: https://reccloud.com/u/bcuhl5y
DECANTAÇÃO
- Separar sólidos depositados num líquido.
- Consiste em transferir o líquido para outro recipiente através de uma vareta.
exemplo: mistura de água e areia.
vídeo Escola Virtual: https://reccloud.com/u/gdc4pr6
DECANTAÇÃO EM FUNIL (ampola de decantação)
- Separar líquidos que não se misturam, isto é, líquidos imiscíveis.
exemplo: água e azeite.
vídeo Escola Virtual: https://reccloud.com/u/m2sg4vc
SEPARAÇÃO MAGNÉTICA
-Separar um componente através da utilização de um íman.
exemplo: separar bolinhas de ferro de areia
vídeo Escola Virtual: https://reccloud.com/u/3rz5qnl
EXTRACÇÃO POR SOLVENTE
- Utiliza-se quando um dos componentes sólidos é solúvel num solvente.
nota: a seguir faz-se uma decantação para separar a fase líquida da fase sólida.
exemplo: separar o açúcar da água numa solução de água doce.
SUBLIMAÇÃO
Separar um componente que sublima facilmente através do aquecimento.
exemplo: mistura de iodo e areia
PENEIRAÇÃO
Separar componentes sólidos formados por partículas de tamanhos diferentes.
exemplo: separar uma mistura de areia e pedras.
vídeo Escola Virtual: https://reccloud.com/u/51vubd2
DESTILAÇÃO SIMPLES
- Separar sólidos dissolvidos em líquidos.
exemplo: obter água "doce" a partir da água do mar (processo usado em países com falta de recursos hidrícos para consumo humano).
vídeo Escola Virtual: https://reccloud.com/u/62k1biw
DESTILAÇÃO FRACCIONADA
- Separar líquidos miscíveis com pontos de ebulição muito diferentes.
exemplo: separação da gasolina, gasóleo, óleos, querosene e outros a partir do petróleo (ver imagem pág. 152 do manual).
vídeo Leya: https://reccloud.com/u/o8g70j5
CROMATOGRAFIA
- Separar substâncias diferentes que percorrem distâncias diferentes ao longo de uma tira de papel ou uma placa própria de material poroso, por um solvente apropriado.
exemplo: separar os corantes constituintes de uma mistura.
vídeo da Escola Virtual: https://reccloud.com/u/jflvdum
VAPORIZAÇÃO
- Obter um sólido que está dissolvido num líquido. O sólido é obtido mais rapidamente e não se formam cristais.
- Consiste no aquecimento da solução para que ocorra a ebulição do líquido.
exemplo: separar rapidamente o sal da água numa solução aquosa de água salgada, mas de
CRISTALIAZAÇÃO ou EVAPORAÇÃO DO SOLVENTE
- Obter um sólido sob a forma de cristais que está dissolvido num líquido.
- Os cristais são obtidos através da evaporação lenta do líquido (evaporação do solvente).
exemplo: obtenção do sal de cozinha (utilizamos para cozinhar) nas salinas.
vídeo da escola virtual: https://reccloud.com/u/ahgi12z
4-Escreve no caderno diário os procedimentos para uma possível solução dos crimes seguintes:
4.1- Encontrou-se um homem morto junto à foz do rio ave. Verificou-se na autópsia que a causa da morte foi afogamento (tinha água nos pulmões).
Mas a polícia tem dúvidas quanto ao local onde efetivamente ocorreu o afogamento: no mar ou no rio?
Como poderias a ajudar a responder à dúvida da polícia?
Apresenta a tua resposta de acordo com a informação apresentada e baseada em conhecimentos científicos.
4.2- Na construção de uma casa ocorreu um acidente: esta ruiu quando foi dada por terminada.
O construtor afirma que utilizou todos os materiais previstos no projeto da casa.
Mas o dono afirma que o construtor em vez de usar vigas de ferro utilizou vigas de alumínio e que, por isso, a estrutura cedeu e caiu.
O caso foi a tribunal e o juiz tinha de saber a quem dar razão.
Como poderias a ajudar o juiz a decidir corretamente?
Apresenta a tua resposta de acordo com a inforção apresentada e baseada em conhecimentos científicos.
SÃO CARACTERÍSTICAS ÚNICAS DE CADA SUBSTÂNCIAS (NAS MESMAS CONDIÇÕES).
ESTAS CARACTERÍSTICAS NÃO DEPENDEM DA FORMA NEM DO TAMANHO DA AMOSTRA CONSIDERADA.
Manual 7º ano: páginas 134 até 141 + página 145
MASSA VOLÚMICA ou DENSIDADE:
é a relação entre a massa de um corpo e o volume ocupado por este chamamos de massa volúmica (densidade).
A massa volúmica ou densidade representa-se por (ρ), expressa-se em g/cm3 (ou g/ ml) e calcula-se da seguinte forma:
ρ = m / V
Cada substância tem um único valor de massa volúmica. (ver tabela pág. 135 do manual)
Consultando a tabela da página 135 do manual responde às seguintes questões:
1- Se juntasse água e alumínio quem "afundava": a água ou o alumínio? Justifique com base nos dados da tabela.
2- Se juntasse água e gasolina quem "afundava": a água ou a gasolina? Justifique com base nos dados da tabela.
PONTO DE EBULIÇÃO:
é a temperatura a que a substância passa do estado LÍQUIDO para o estado GASOSO de forma rápida e tumultuosa (ebulição), a uma dada pressão.
Cada substância tem um único valor de ponto de ebulição. (ver tabela pág. 139 do manual)
Consultando a tabela dos pontos de ebulição da página 139 do manual responde às seguintes questões:
1- Como se chama a substância que entra em ebulição à temperatura de 78 ºC ?
2- A que temperatura é que a água começa a entrar em ebulição?
3- Qual das três substâncias da tabela é a mais VOLÁTIL, isto é, passa com maior "facilidade" do estado líquido para o estado gasoso?
PONTO DE FUSÃO:
é a temperatura a que a substância passa do estado sólido para o estado líquido (funde), a uma dada pressão.
Cada substância tem um único valor de ponto de fusão. (ver tabela pág. 138 do manual)
Consultando a tabela dos pontos de fusão da página 138 do manual responde às seguintes questões:
1- Como se chama a substância que começa a fundir à temperatura de 660 ºC ?
2- Como se chama a substância que começa a passar do estado sólido ao estado líquido à temperatura de 1540 ºC?
3- Se encontrasse um pedaço de metal e quisesse saber se era de chumbo, aluminio ou cobre, o que poderia fazer para descobrir?
3- Preparam-se 3 soluções de água salgada:
A- 6 gramas de sal dissolvido em 3 cm3 de solução.
B- 9 gramas de sal dissolvido em 3 cm3 de solução.
C- 3 gramas de sal dissolvido em 3 cm3 de solução.
3.1- Como se chama a substância que funciona como solvente?
3.2- Qual é o valor da concentração mássica de cada uma das soluções?
3.3- Qual é a solução menos concentrada?
3.4- Porque podemos dizer que são todas soluções aquosas?
Uma forma de exprimir a relação das quantidades de soluto e solvente é através da concentração da solução.
Uma forma de exprimir quantitativamente a relação das quantidades de soluto e solvente é através da concentração mássica.
concentração mássica é igual ao quociente entre a massa do soluto e o volume da solução, isto é,
Concentração mássica = massa do soluto / volume da solução
massa do soluto pode exprimir- se em gramas (g)
volume da solução pode exprimir-se em centímetros cúbicos (cm3)
nota: considerar que 1 cm3 é igual a 1 mL
Concentração qualitativa pode ser definida através de processos colorimétricos, isto é, análise qualitativa da cor da solução.
Se considerarmos uma solução colorida, podemos dizer que quanto mais intensa for a cor da solução maior é a concentração da solução.
O problema deste método é que não funciona em soluções incolores ( como por exemplo água com açúcar).
Então como fazer?
Classifica as seguintes misturas:
aço:
água salgada:
ouro de ourivesaria:
maionese:
pizza:
água com areia:
tosta mista:
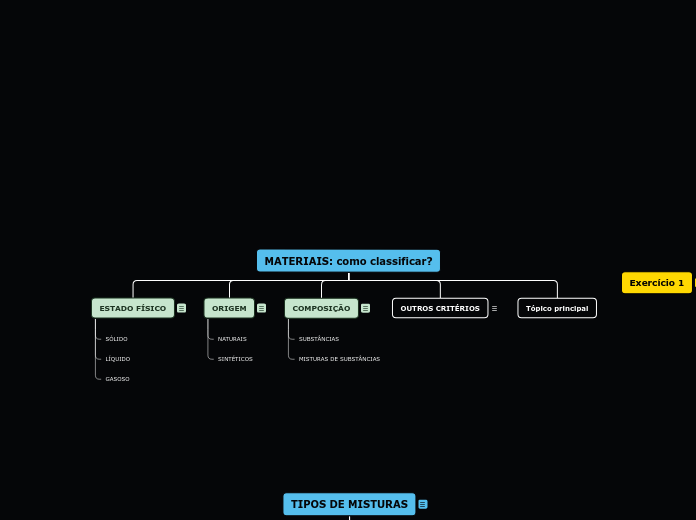
Consultando as páginas 94, 95 e 100 do teu manual classifica os seguintes materiais quanto à sua:
COMPOSIÇÃO:
ar:
granito:
água mineral:
água do mar:
ferro:
tosta mista:
ORIGEM:
rocha de granito:
plástico:
medicamentos:
pepita de ouro:
ar:
calças:
ESTADO FÍSICO:
ar:
granito:
água mineral:
água do mar:
prego de ferro:
açúcar:
plástico:
ouro de um anel:
gasolina:
Solvente: substância que dissolve o soluto.
exemplo: água salgada:
a água é o solvente porque dissolve o sal.
Soluto: substância que é dissolvida pelo solvente.
exemplo: água salgada
o sal é o soluto porque é dissolvido pela água.
As misturas podem ser classificadas quanto à forma como as substâncias constituintes estão distribuídas na mistura.
vídeo: https://reccloud.com/u/t1a9ocs
Os componentes da mistura não se distinguem a olho nu (aspeto homogénea), mas distinguem-se ao microscópio (aspeto heterogéneo).
Tintas
Maionese
Sangue
Leite
Gelatina
Guache
MAnteiga
Ketchup
Iogurte
A composição da mistura é uniforme.
Os componentes da mistura não se distinguem a olho nu, nem ao microscópio.
São também designadas de soluções.
Ar (sem poeiras)= azoto + oxigénio + dióxido de carbono + ...
Álcool etílico = água + etanol
Aço = ferro + carbono
A composição da mistura não é uniforme.
Os componentes da mistura distinguem-se a olho nu.
Coca-cola = gás + líquido
granito
areia + água
azeite+ água
Também podem haver classificações de materiais considerando a sua cor ou a sua textura.
Os materiais também podem ser classificados quanto ao reino de onde provêm: Reino Animal Reino Vegetal Reino Mineral
Outros critérios como metal/ não metal, etc...
Os materiais podem ser classificados quanto à sua composição, isto é, se têm uma substância ou várias substâncias.
Se o material tiver apenas uma a substância: SUBSTÂNCIA.
Se o material tiver mais do que uma substância: MISTURA DE SUBSTÂNCIAS.
Classifique os materiais seguintes relativamente à sua composição.
ar
oxigénio
petróleo bruto
granito
ouro de um anel
água mineral
água da torneira
água destilada
dióxido de carbono
pizza
coca-cola
chocolate
Os materiais podem ser classificados quanto à sua origem, isto é, a sua proveniência (de onde vêm).
É tentar classificá-los se são usados tal qual vêm da natureza- NATURAIS, ou se são produzidos fabricados pelos seres humanos- SINTÉTICOS ou FABRICADOS.
Classifica os seguintes materiais quanto à sua origem:
ar
rochas
plástico
medicamentos
mesa
árvore
maçã
camisola de lã
seda
Todos o materiais podem ser classificados quanto ao seu estado físico: Sólido, Líquido ou Gasoso.
vídeo: https://reccloud.com/u/cwkf2r8